Vergelijkingen van het immunologische landschap tussen patiënten met COVID-19,influenza en respiratoir syncytieel virus door middel van clusteranalyse
Jun 15, 2022
Neem voor meer informatie contact op metdavid.wan@wecistanche.com
a b s t r a c t
Achtergrond: COVID-19 heeft sterker besmettelijkheid en a hoger risico voor ernst dan meest ander besmettelijke luchtwegen ziektes. De mechanismen onderliggende deze verschil blijven onduidelijk.
Methoden:: Wij vergeleken de immunologisch landschap tussen COVID-19 en twee ander besmettelijk respiraterij ziektes (influenza en ademhalings syncytieel virus (RSV)) door clustering analyse van de drie dis-versoepelt gebaseerd Aan 27 immuun handtekeningen' scoort.
Resultaten: Wij identified drie immuun subtypes: Immuniteit-H, Immuniteit-M, en Immuniteit-L, welke dis-gespeeld hoog, medium, en laag immuun handtekeningen, respectievelijk. Wij gevonden20 procent, 35,5 procent,en44,5 procent van COVID-19 gevallen inbegrepen in Immuniteit-H, Immuniteit-M, en Immuniteit-L, respectievelijk; allemaal influenza gevallen waren: inbegrepen in Immuniteit-H; 66,7 procenten33,3 procentvan RSV gevallen behoorde tot tot Immuniteit-H en Immuniteit-L,respectievelijk. Deze gegevens aangeven Dat meest COVID-19 patiënten hebben zwakker immuun handtekeningen dan influenza en RSV patiënten, net zo bewezen door 22 van de 27 immuun handtekeningen hebben lager verrijkingsscores in COVID-19 dan in influenza en/of RSV. De Immuniteit-M COVID-19 patiënten had de hoogste uitdrukking niveaus van ACE2 en IL-6 en laagste viraal ladingen en waren de jongste. In contrast, de immuniteit-H COVID-19 patiënten had de laagste uitdrukking niveaus van ACE2 en IL-6 en hoogste viraal ladingen en waren de oudste. Meest immuun handtekeningen had lager verrijking niveaus in de intensief zorg eenheid(ICU) dan in niet-ICU patiënten. Gen ontologie analyse liet zien Dat de aangeboren en aangepaste immuunreacties waren signifischuin gedownreguleerd in COVID-19 versus gezond individuen.
conclusies: Vergeleken tot influenza en RSV, COVID-19 weergegeven signifischuin verschillend immunologiecali profiles. Verhoogd immuun handtekeningen zijn geassocieerd met a beter prognose in COVID-19 patiënten.
@ 2021 De Auteur(s). gepubliceerd door Elsevier B.V. Aan namens van Onderzoek Netwerk van rekenkundig en structureel Biotechnologie. Deze is een vrije toegang artikel onder de CC DOOR-NC-ND licentie


Klik hier voor meer informatie over Cistanche
1. Achtergrond
De coronavirus ziekte 2019 (COVID-19) veroorzaakt door de ernstig acuut ademhalings syndroom coronavirus 2 (SARS-CoV-2) heeft gemeld tot overschrijden 126 miljoen gevallen en resulteerde in in meer dan2.7 miljoen sterfgevallen wereldwijd net zo van Maart 26, 2021 [1]. COVID-19aandelen vergelijkbaar klinisch presentaties met influenza en respiratoire syncytiële virus (RSV), zo een net zo hoesten, koorts, erge, ernstige long infecties,en af en toe ademhalings mislukking veroorzaken sterfgevallen [2], niettemin,COVID-19 heeft ook gedemonstreerd verschillend klinisch kenmerken,
zo een net zo gastro-intestinaal ongemak, zenuw verwondingen, en hypogeusie[3,4]. Vergeleken tot ander besmettelijk ademhalings ziektes, zo een als influenza en RSV, COVID-19 heeft sterker besmettelijkheid en a hoger -risico voor ernst, zo een net zo ademhalings angst en systematische inflammatie [3,5]. Meer ernstig, COVID-19 vaak heeft a lange incubatie periode Dat signifischuin neemt toe zijn overdraagbaarheid[3,5,6]. in tegenstelling tot veel ander ademhalings virussen, SARS-CoV-2 besmettenties kunnen resultaat in gastheer hyperinflliefdesverdriet antwoord, gekarakteriseerd door a hoog niveau van circulerend inflliefdesverdriet cytokinen en interleukine-6 (IL-6) [7]. Meerdere studies hebben getoond Dat a grote hoeveelheid van type I interferon gepromoveerd inflliefdesverdriet cytokinen productie en resulteerde in in dodelijk longontsteking [8,9]. Immuun dysfunctieties is ook a karakteristiek van COVID-19 [10]; net zo getoond in ernstige COVID-19 gevallen, de totaal nummers van T en B cellen zijn verminderd,resulterend van overgeproduceerd pro-inflliefdesverdriet cytokinen [11].Tot ontdekken potentieel mechanismen onderliggende de signifikan niet anders zijn klinisch kenmerken van COVID-19, wij vergeleken de immunologische landschap tussen COVID-19, influenza, en RSV gebaseerd Aan hun gen uitdrukking profiles. Wij uitgevoerd a clusteranalyse tot identificeren immuun subtypes van COVID-19, influenza, en RSV gebaseerd Aan de verrijking niveaus van 27 immuun handtekeningen. We identificeerden drie immuun subtypes met hoog, medium, en laag immuunsysteem handtekeningen, respectievelijk, en ontleed deze subtypes'moleculair Kenmerken. Wij ook verkend correlaties tussen deze immuun handtekeningen en verscheidene klinisch kenmerken in COVID- 19 patiënten. Deze studie gericht tot voorzien in nieuwe inzichten naar binnen de immunologische landschap van COVID-19.

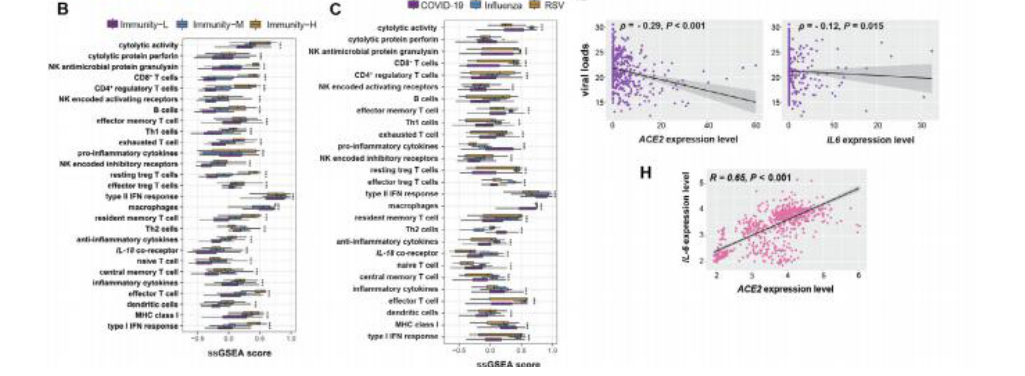

Afb. 1. identiteitfikation van immuun subtypes van COVID-19, influenza, en RSV. (A) Hiërarchisch clustering opbrengsten drie subtypes: Immuniteit-H, Immuniteit-M, en Immuniteit-L,
gebaseerd Aan de verrijking scoort van 27 immuun handtekeningen. (B) vergelijkingen van de verrijking scoort van 27 immuun handtekeningen tussen de drie immuun subtypes. (C)vergelijkingen van de verrijking scoort van 27 immuun handtekeningen tussen COVID-19, influenza, en RSV patiënten. (D) vergelijkingen van de uitdrukking niveaus van ACE2 en IL-6tussen de drie immuun subtypes en tussen de drie immuun subtypes bevattende COVID-19 enkel en alleen. (E) vergelijkingen van COVID-19 patiënten' leeftijden tussen de drie immuun subtypes. (F) vergelijkingen van viraal ladingen in COVID-19 patiënten tussen de drie immuun subtypes. (G) Speerman correlatie tussen de uitdrukking niveaus vanACE2en IL-6 en viraal ladingen in COVID-19 patiënten. (H) Pearson correlatie tussen de uitdrukking niveaus van ACE2 en IL-6 in COVID-19 patiënten. * P< 0.05, **P< 0.01, ***P< 0.001.
2. Methoden:
2. 1. Gegevenssets
Wij verzameld acht gen uitdrukking profileng datasets, inclusief
vier COVID-19 RNA-volgende datasets [12-15], een RSV RNA-volgende dataset van de Gen Uitdrukking Omnibus database (GEO, https://www. ncbi.nlm.NIH.regering/geo-/), een RSV microarray gegevensset [16], een influenza microarray gegevensset van GEO, en een microarray gegevensset voor beide RSV en influenza [17] (Tafel 1). Eerst, wij verzameld rauw data van deze datasets, samengesteld van 1,036 patiënten en 273 gezond controllen. De 1,036 patiënten inbegrepen 842 COVID-19, 44 influenzas,en 150 RSV patiënten. De mediaan- leeftijd van deze patiënten was53 jaar (interkwartiel bereik: 38–67 jaar). Tussen deze patiënten, 404 (38,96 procent)waren vrouwen, 348 (33,61 procent)waren mannen, en 284 (27,43 procent)waren niet geïdentificeerdfied. Daar waren 100 COVID-19 gevallen in de gegevensset GSE157103, inclusief 50 intensief zorg eenheid (ICU) gevallen en 50 niet-ICU gevallen. De vier COVID-19 datasets inbegrepen
patiënten van de Verenigde Staten van Amerika. De twee influenza datasets opgenomen patiënten van Canada en de VK, respectievelijk, en de twee RSV-gegevenssets inbegrepen patiënten van de VK en de Verenigde Staten van Amerika. De patiënten'weefsels in deze datasets is ontstaan van de bovenste luchtwegen, perifeereral bloed mononucleair cellen, leukocyten, en bloed. Volgende, wij pergevormd a kwaliteit controle analyse tot detecteren uitbijters in elk dataset met behulp van WGCNA [7]. Eindelijk, wij samengevoegd deze datasets gebruik makend van de''samenvoegen" functie in de R pakket ''baseren" en uitgevoerd de aanpassing van partij Effecten en normalisatie van de gecombineerde gegevens gebruik makend van de ''normaliseren tussen arrays" functie in de R inpakkenleeftijd ''lima. " Omdat deze studie gericht tot vergelijken immuun signatures tussen COVID-19, influenza, en RSV, de bacterieel en andere anoniem virussen-geassocieerd monsters waren uitgesloten.
2.2. Clustering
Wij uitgevoerd een uitgebreid literatuur zoeken voor immuun signatures geassocieerd met ademhalings virus infectie en verzameld27 immuun handtekeningen erbij betrekken 136 markeerstift genen [18-21]. Wijfieerst kwantitatieffied de verrijking niveaus van de 27 immuun handtekeningen in elk steekproef door de enkel-steekproef gen-set verrijking analyse(ssGSEA) [22]. Gebaseerd Aan de ssGSEA scoort van de 27 immuun signatures, wij uitgevoerd hiërarchisch clustering van de monsters in de samenvoeging gegevensset gebaseerd Aan de Euclidische statistieken.
2.3. Gen-set verrijking analyse
Wij identified gen ontologie (GAAN) en KEGG paden upregu-
laat en gedownreguleerd in COVID-19, influenza, RSV, en hun
immuun subtypes door GSEA [23] (R implementatie) met a dorsenoud van bijgestelde P-waarde< 0.05.
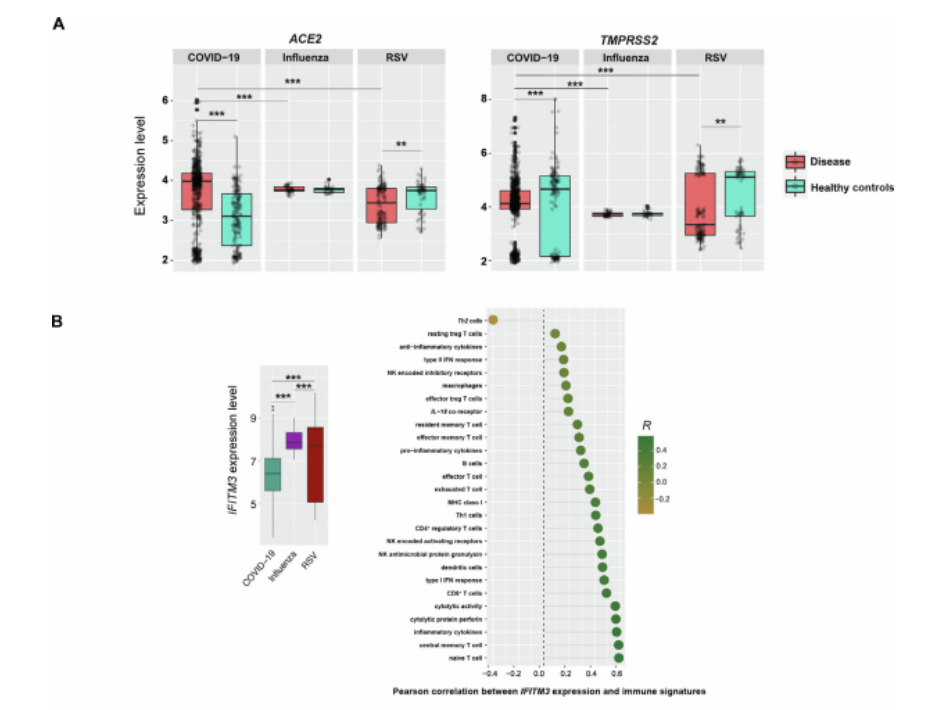


Afb. 2. identiteitfikation van differentieel uitgedrukt genen en gen ontologie (GAAN) tussen COVID-19 patiënten en influenza en RSV patiënten. (A) vergelijkingen van de expressieniveaus van ACE2 en TMPRSS2 tussen virus-besmet patiënten en gezond controles. (B) IFITM3 shows signifischuin lager uitdrukking niveaus in COVID-19 dan in influenza en RSV patiënten en krachtig positief uitdrukking correlaties met immuun-promoten handtekeningen. GAAN termen opgereguleerd en gedownreguleerd in COVID-19 (C), influenza (D), en
RSV (E) patiënten versus gezond controles. (F) GAAN termen zeer verrijkt in COVID-19 versus influenza. * P< 0.05, **P< 0.01, ***P< 0.001.
2.4. identiteitfikation van gen modules verrijkt in immuun subtypes
Wij gebruikt WGCNA [7] tot identificeren gen modules signifinauwelijks verrijkt in immuun subtypes gebaseerd Aan gen co-uitdrukking netto-werk analyse. Gebaseerd Aan de uitdrukking correlaties tussen het gen modules' middelpunt genen, wij identified de GAAN termen signifikan niet gecorreleerd zijn tot specific onderscheidende kenmerken.
2.5. Statistisch analyse
In de vergelijking van verschillend groepen van gegevens, wij gebruikt Leerling's t-testen of ANOVA testen als zij waren normaal gesproken gedistribueerd; anders,wij gebruikt de Mann–Whitney U testen of Kruskal–Wallis testen. Wij gebruikte de Pearson correlatie coeffiwetenschappelijk (R) tot evalueren de expressie correlatie tussen twee genen en de Speerman correlatie coeffiwetenschappelijk (p) tot schatten correlaties tussen ander variabelen. wij hebben aangepast P waarden in meerdere testen gebruik makend van de vals ontdekking tarief(FDR), welke was berekend door de Benjamini-Hochberg methode.Wij uitgevoerd allemaal statistisch analyseert gebruik makend van R programmeren (versie 4.0.2).
3. Resultaten
3. 1. De immuun subtypes van COVID- 19, influenza, en RSV
Gebaseerd Aan de 27 immuun handtekeningen' verrijking scoort, wij hiërarchisch geclusterd de 809 virus-besmet geduldig op monsters gebaseerd Aan de Euclidische afstand metriek. Wij verkregen drie Doorzichtig
clusters, genoemd Immuniteit-H, Immuniteit-M, en Immuniteit-L,welke weergegeven de hoogste, medium, en laagste immuun handtekening niveaus, respectievelijk (Afb. 1A). In feit, tussen de 27 immuun handtekeningen, 21 weergegeven signifischuin hoger verrijking scoort in immuniteit-H dan in Immuniteit-M en Immuniteit-L (een-manier ANOVA testen, P< 0.05) (Afb. 1B). Wij gevonden20 procent, 35,5 procent,en44,5 procentvan COVID-19 gevallen inbegrepen in Immuniteit-H, Immuniteit-M, en immuniteit-L, respectievelijk; allemaal influenza gevallen waren inbegrepen Immuniteit-H; 66,7 procenten33,3 procentvan RSV gevallen behoorde tot Immuniteit-H en Immuniteit-L, respectievelijk. Deze resultaten indicate Dat meest COVID-19 patiënten hebben zwakker immuun handtekeningen dan de patiënten besmet met ander virussen. Deze was bewezen doordeDat 22 van de 27 immuun handtekeningen weergegeven lager verrijkenment scoort in COVID-19 dan in influenza en/of RSV patiënten(Afb. 1C).
Angiotensine-converteren enzym 2 (ACE2) is de gastheer cel receptor van SARS-CoV en SARS-CoV-2 [3]. Wij gevonden Dat ACE2 expressie niveaus waren de hoogste en laagste in Immuniteit-M en immuniteit-H, respectievelijk (twee-staart Leerling's t-testen, P< 0.05) (Afb. 1D). IL-6 heeft geweest aangegeven net zo een nadelig voorspeller van COVID-19. Opmerkelijk, de uitdrukking niveaus van IL-6 waren de hoogste en laagste in Immuniteit-M en Immuniteit-H, respectievelijk(P< 0.05) (Afb. 1D). Wanneer de gevallen van influenza en RSV werden uitgesloten, de uitdrukking niveaus van ACE2 en IL-6 waren nog altijd de hoog-Est en laagste in Immuniteit-M en Immuniteit-H, respectievelijk(P< 0.05) (Afb. 1D). Het aangegeven Dat de COVID-19 gevallen in immuniteit-M en Immuniteit-H kunnen hebben verschillend prognoses.Inderdaad, de COVID-19 patiënten waren de jongste en oudste in immuniteit-M en Immuniteit-H, respectievelijk (Kruskal–Wallis testen, P = 0.003) (Afb. 1E). Bovendien, de COVID-19 patiënten had de laagEst en hoogste viraal ladingen in Immuniteit-M en Immuniteit-H,respectievelijk (P = 0.004) (Afb. 1F). De uitdrukking niveaus van ACE2en IL-6 waren omgekeerd gecorreleerd met viraal ladingen in COVID-19patiënten (Speerman correlatie, p = — 0.29, P< 0.001,p = — 0.12, P < 0.015,="">respectievelijk) (Afb. 1G). In de tussentijd, wij opgemerkt a sterke uitdrukking correlatie tussen ACE2 en IL-6 in COVID-19patiënten (Pearson correlatie R = 0.65, P< 0.001) (Afb. 1H).
Algemeen, deze resultaten aangeven Dat de gastheer immuun antwoord naar SARS-CoV-2 infectie is aannemelijk tot zijn meer zwaar ontregeld dan de antwoord tot de ander virussen' infectie.


Afb. 3. Gen modules verrijkt in immuun subtypes en ziekten. 12 gen modules (aangegeven in turkoois, groente, Purper, bruinen, magenta, geel, blauw, bruin, zwart, roze,groente-geel, en rood kleuren) signifischuin gedifferentieerd deze patiënten door immuun subtype (A) en ziekte (B) identified door WGCNA. De vertegenwoordiger gen ontologie (GAAN)voor gen modules, correlatie coefficienten, en P waarden (in haakjes) zijn getoond. DeGrijs module bevat niet toegewezen genen en heeft nee GAAN geassocieerd met het. (Voor interpretatie van de referenties tot kleur in deze figoeroe legende, de lezer is verwezen tot de web versie van deze artikel.) (Voor interpretatie van de referenties tot kleur in dezefigoeroe legende, de lezer is verwezen tot de web versie van deze artikel.)
3.2. differentieel uitgedrukt genen en paden tussen COVID- 19patiënten en influenza en RSV patiënten
ACE2 en TMPRSS2 zijn twee cruciaal moleculen voor SARS-CoV-2binnenvallen gastheer cellen [24]. Wij gevonden Dat ACE2 uitdrukking niveaus waren signifischuin hoger in COVID-19 patiënten dan in gezondcontroles, influenza, en RSV patiënten (P< 0.05) (Afb. 2A). TMPRSS2uitdrukking niveaus waren signifischuin lager in COVID-19 patiënten dan in gezond controles, terwijl het was signifischuin hoger in COVID-19 patiënten dan in influenza en RSV patiënten (P< 0.05) (Afb. 2A). Verder, wij identified 41 genen laten zien signifischuin verschillend uitdrukking niveaus tussen COVID-19 patiënten en gezond controles (FDR< 0.1,vouwen Wijzigen groter dan 2). Onder hen, 12 genen codering transcriptioneel factoren (TF's) waren upregulated in COVID-19 patiënten. De 12 TF's inbegrepen five viraal replicaties en mobiel antwoord remmers (ALS HET3, DDX58, MX1, OAS1, en TRIM22), een chemokine (CXCL10), twee interferon-gamma signaal-ing bemiddelaars (XAF1 en GBP1), een macrofaag activering moduleraar (EPSTI1), twee immuun antwoord modulatoren (STAT1 en EIF2AK2), en een interferon's antiviraal werkzaamheid modulator(IFITM3). In influenza en RSV patiënten, 14 en 40 TF genen werden opgereguleerd familielid tot hun gezond controles, respectievelijk. IFITM3was de enkel en alleen TF gen algemeen opgereguleerd in COVID-19, influen-za, en RSV patiënten. Echter, IFITM3 had signifischuin lagere uitdrukking niveaus in COVID-19 dan in influenza en RSV patiënten en liet zien krachtig positief uitdrukking correlaties met immuun handtekeningen (Afb. 2B). Opnieuw, deze resultaten aangeven de verschillen in gastheer immuun antwoord in COVID-19 versus influenza en RSV-patiënten.
GSEA identified 81 GAAN termen verrijkt in COVID-19 patiënten,welke waren voornamelijk betrokken in de regulatie van metabolisme,extracellulair Matrix, Tol-Leuk vinden receptoren (TLR's), nijlpaard signalering,en immuun antwoord. In contrast, twee GAAN termen betrokken in reg ubiquitine en aangeboren immuniteit waren gedownreguleerd in
COVID-19 patiënten (Afb. 2C). In toevoeging, GSEA identified 272 GO-voorwaarden verrijkt in influenza patiënten, meest van welke waren betrokken bij de regulatie van inflliefdesverdriet en immuun reacties (Afb. 2D). 49 GAAN termen waren verrijkt in RSV patiënten, meest van welke waren geassocieerd met immuun regulatie (Afb. 2E). Verrassend genoeg, geen van deze GAAN termen waren algemeen opgereguleerd of gedownreguleerd onder de drie groepen van virus-besmet patiënten, uniek aangeven moleculair wijzigingen in elk groep van virus-geïnfecteerde patiënten.
Wij ook uitgevoerd a vergelijking van gen uitdrukking profiles tussen de COVID-19 patiënten en influenza en RSV patiënten.Wij gevonden 126 GAAN termen zeer verrijkt in COVID-19, meest van welke waren betrokken in de regulatie van metabolisme, chemokinen,en cytokinen. In toevoeging, 32 GAAN termen waren gedownreguleerd in COVID-19, welke waren voornamelijk geassocieerd met genomisch stabiliteitsregeling (Afb. 2F en Aanvullend Afb. S1A). Daarnaast, wij com-gepareerd gen uitdrukking profiles tussen Immuniteit-H, Immuniteit- M, en Immuniteit-L. Wij gevonden 107 GAAN termen signifischuin upreguverjaard in Immuniteit-H versus Immuniteit-L, en 136 GAAN termen betekenisvolkortom opgereguleerd in Immuniteit-M versus Immuniteit-H (Aanvullend Afb. S1B, C, D). Net zo verwacht, deze GAAN termen waren voornamelijk betrokken in de regulatie van de immuun systeem. Collectieftief, deze resultaten aangeven Dat de gastheer immuun antwoord naar SARS-CoV-2 is signifischuin verschillend van Dat van de ander virussen en Dat SARS-CoV-2 infectie kunnen beïnvloeden de van de gastheer metabolisch proophouden en genomisch stabiliteit.


Afb. 4. verenigingen tussen immuun handtekeningen en klinisch Kenmerken in COVID-19 patiënten. (A) vergelijkingen van de verrijking niveaus van 27 immuun handtekeningen tussen IC en niet-ICU gevallen. Twee-staart Leerling's t-testen P waarden zijn aangegeven. (B) Heatmap laten zien Speerman correlaties tussen de verrijking niveaus van 27 immuun handtekeningen en klinisch parameters in COVID-19. * P< 0.05, **P< 0.01, ***P< 0.001.De resultaten in (A, B) waren verkregen door analyseren de gegevensset GSE157103.
3.3. Gen modules verrijkt in immuun subtypes en ziekten
Wij gebruikt WGCNA [7] tot identificeren vergelijkbaar co-uitdrukking genmodules Dat gedifferentieerd patiënten door subtype (Immuniteit-H,Immuniteit-M, en Immuniteit-L) of ziekte (COVID-19, influenza,en RSV). Wij identified 12 gen modules gemarkeerd in verschillende kleuren: turkoois, groente, Purper, bruinen, magenta, geel, blauw, bruin,zwart, roze, groente-geel, en rood (Afb. 3A). Net zo verwacht, het immuunsysteem antwoord, a vertegenwoordiger GAAN termijn voor de geel module,was zeer verrijkt in Immuniteit-H versus Immuniteit-M en immuniteit-L (r = 0.26, P = 4.0 x 10 — 14 ). De viraal transcriptiewas ook zeer verrijkt in Immuniteit-H (r = 0.77, P = 3.0 x 10 — 160 ), terwijl het was verarmd in Immuniteit-M (r = —0.28, P = 2 .0 x 10 — 16 ) en Immuniteit-L (r = —0.47, P = 2.0 x 10 —46 ). Het is echt-
redelijk omdat hoog niveaus van viraal replicatie kunnen oorzaak a sterkger gastheer immuun antwoord. De extracellulair Matrix was zeer verrijkt in Immuniteit-M (r = 0.47, P = 2.0 x 10 —46 ), terwijl het werd gedownreguleerd in Immuniteit-H (r = —0.52, P = 1.0 x 10 —57 ). De verdediging antwoord tot virus was ook opgereguleerd in Immuniteit-M (r = 0.12, P = 5.0 x 10 —4 ), terwijl het was gedownreguleerd in immuniteit-L (r = —0.15, P = 1.0 x 10 —5 ) en liet zien nee signifikan geen correlatie met Immuniteit-H (r = 0.045, P = 0.2). Het aangegeven die immuniteit-M en Immuniteit-L had de sterkste en zwakste verdediging antwoord tot virus infectie tussen de drie subtypes.De epitheel cel proliferatie was zeer verrijkt in Immuniteit- L en Immuniteit-M, terwijl het was gedownreguleerd in Immuniteit-H.
Insgelijks, WGCNA identified 12 gen modules Dat signifiniet goed gedifferentieerd deze patiënten door ziekte (COVID-19, influenza, en RSV) (Afb. 3B). Opmerkelijk, tien gen modules weergegeven hoger verrijkenment in COVID-19 familielid tot influenza en RSV. interessant genoeg, het immuunsysteem antwoord was zeer verrijkt in COVID-19 versus influenza en RSV (r = 0.46, P = 8.0 x 10 —44 ). De verdediging antwoord virus maken was ook verrijkt in COVID-19 vergeleken tot influenza en RSV (r = 0.1, P = 0.004). Het suggereert Dat COVID-19 patiënten heb een sterker immuun antwoord tot virus infectie dan influenza en RSV patiënten, welke kunnen zijn beschreven net zo een inflliefdesverdriet antwoord op antigeen stimulus. In toevoeging, twee gen modules voor welke representatief GAAN termen waren kern en chromosoom, respectievelijk,waren signifischuin opgereguleerd in COVID-19. In contrast, de virale transcriptie was signifischuin gedownreguleerd in COVID-19 versus influenza en RSV (r = —0.72, P = 6.0 x 10 — 127 ).
3.4. verenigingen tussen immuun handtekeningen en klinisch Kenmerken in
COVID- 19 patiënten
Wij verder geanalyseerd verenigingen tussen de 27 immuun sigaard en klinisch Kenmerken in COVID-19 patiënten in GSE157103.De klinisch Kenmerken inbegrepen ICU, de acuut Fysiologie en chronisch Gezondheid Evaluatie (APACHE II), de sequentieel Orgaan Mislukkingure Beoordeling (BANK), Charlson scoren, C-reactief Eiwit (CRP), D-dimeer, ferritine, fibrinogen, ziekenhuis vrij dagen (45 dagen volgen-omhoog), melk geven, procalcitonine, en ventilator-vrij dagen. Beide APACHE II en BANK scoort meeteenheid de ernst van ICU patiënten [25]. De Charlson scoren voorspelt de tien-jaar sterfte voor a geduldig met een bereik van comorbide conditie [26]. De CRP, D-dimeer, ferritine, fibrinogeen, melk geven, en procalcitonine zijn laboratorium metingen waarvan? hoog niveaus waren gecorreleerd met de ernst van COVID-19 [27]. Opmerkelijk, wij gevonden Dat 20 immuun handtekeningen had signifischuin lager verrijking niveaus (ssGSEA scoort) in ICU dan in niet-ICU patiënten (P< 0.05) (Afb. 4A). Enkel en alleen twee immuun handtekeningen(type II IFN antwoord en inflliefdesverdriet cytokinen) had signifikan niet hoger ssGSEA scoort in ICU dan in niet-ICU patiënten. Bovendien,meest van deze immuun handtekeningen' ssGSEA scoort waren negatief gecorreleerd met de niveaus van CRP, D-dimeer, ferritine, fibrinogen, melk geven, en procalcitonine (Afb. 4B). In contrast, a meerderheid van deze immuun handtekeningen' ssGSEA scoort waren positief gecorreleerd met ziekenhuisvrijdagen en ventilator-vrij dagen. collectief, deze resultaten stel voor Dat verhoogd immuun handtekeningen zijn aannemelijk tot geassocieerd zijn met a beter prognose in COVID-19 patiënten.
4. Discussie en conclusies
Ademhaling traktaat infectie is aansprakelijk voor ongepast ziekte last[28]. De aangeboren en aangepaste immuun reacties tot respiratoir virus infectie zijn kritisch voor in stand houden a gezond ademhalings systeem en voorkomen pulmonaal ziekte [29]. Hoewel COVID-19 aandelen zeker primair symptomen met influenza en RSV [30,31],zijn overdraagbaarheid en vernietigbaarheid ver overschrijden influenza en RSV [1]. De uniek gastheer immuun antwoord in COVID-19 patiënten kunnen enorm bijdrage leveren tot deze ziekte's hoog overdraagbaarheid en vernietigbaarheid [32]. Voor voorbeeld, SARS-CoV-2 infectie mag niet altijd dienst interferon productie maar vertraging of onderdrukken interferon II of III productie in long weefsels [33].
Bij infectie, de influenza virus is erkend door gastheer cellen door pathogeen-geassocieerd moleculair patronen (PAMP's) [34].PAMP's zijn erkend door TLR's, RIG-I, en NLRP3 tot genereren pro-inflliefdesverdriet cytokinen en type I interferon productie, welke heeft krachtig antiviraal werkzaamheid door beperkend virus replicatie in gastheercellen. Type I interferonen kan opwekken STAT activering en transcriptie van de interferon-gestimuleerd gen tot influence aangeboren en adaptief immuun reacties. Verder, gastheer immuun cellen rekruteren alveolair macrofagen tot activeren apoptotisch influenza-virus-besmet cellen, terwijl bloed-afgeleid van macrofagen geïnfecteerd met influenza virussen produceren groot bedragen van pro-inflliefdesverdriet cytokinen [34]. RSV infectie lokt uit a krachtig aangeboren immuunsysteem antwoord, vooral ademhalings traktaat neutrofiel antwoord[35]. De piek van neutrofiel antwoord vaak stemt ermee in met maxi-mamma klinisch ernst en viraal laden. Echter, omdat RSV infectie kan verminderendenatuurlijk moordenaar (NK) cel graaf tot reguleren de inflliefdesverdriet antwoord, a lager NK cel graaf is gecorreleerd met meer echt infectie [36]. Bij acuut infectie, de adaptief immuunsysteem antwoord tussen RSV patiënten is geactiveerd via rekruterings-cd8plusT cellen tot Doorzichtig virussen. In de tussentijd, B cellen Speel een belangrijke rol in de productie van beschermend antistoffen. RSV infectie ook triggers interferon II productie, welke Toneelstukken a krachtig beschermende rol tegen virus infectie [37]. Ons resultaten gedemonstreerd dat vergeleek tot COVID-19, influenza en RSV patiënten uitgelokt a sterkger aangeboren immuun antwoord, e.g., meer interferonen I productie,macrofagen, NK cellen, en dendritisch cellen. Verder, influenzaen RSV patiënten uitgelokt a sterker aangepaste immuun reactie beschreven door meer B en T cel productie.
Vergeleken tot influenza en RSV, COVID-19 is aannemelijk tot lager weergeven immuun handtekeningen en hoger IFN II productie, leiden naar arm prognose en slechter resultaten. De aangeboren en adaptief immuunsysteem reacties zijn signifischuin lager in COVID-19 dan in de ander virussen-besmet patiënten, terwijl chemoattractant eiwit-1 (IL-6) is opgereguleerd in COVID-19 patiënten. In de tussentijd,wij gevonden Dat pro-inflliefdesverdriet cytokinen waren opmerkelijk hoger in COVID-19 dan in influenza en RSV patiënten. In contrast,anti-inflliefdesverdriet cytokinen waren signifischuin lager in COVID-19patiënten, welke kunnen beschrijven de cytokinen storm tussen COVID- 19 patiënten. interessant genoeg, COVID-19 patiënten weergegeven a hogere expressie van cytolytisch optreden dan de patiënten besmet met de ander virussen. Echter, sinds optreden's belangrijk rol leugens in de cytotoxisch werkzaamheid tegen pathogenen, abnormaal productie van dit eiwit kon zijn aansprakelijk voor weerstand tot de cytotoxische activiteit van NK en CD8plusT cellen. Het heeft geweest getoond Dat doelpathogeen cellen kon dienst verscheidene ontsnappen mechanismen tegen perforine werkzaamheid [38].
De clustering analyse liet zien Dat Immuniteit-M en immuniteit-L gehuisvest80 procentvan COVID-19 patiënten, suggereren dat het meest COVID-19 patiënten hebben een onvoldoende immuun antwoord virus maken infectie. Verder, wij gevonden Dat moleculair en klinische kenmerken waren signifischuin verschillend tussen COVID-19 patiënten in immuniteit-M en Immuniteit-H. Voor voorbeeld, Immuniteit-M patiënten hadden signifischuin hoger uitdrukking niveaus van ACE2 en IL-6 terwijl lager viraal ladingen dan Immuniteit-H patiënten. Immuniteit-M patiënten waren jonger dan Immuniteit-H patiënten. De lager viraal ladingen in immuniteit-M dan in Immuniteit-H patiënten kon uitleggen waarom de voormalige had a zwakker immuun antwoord dan de laatstgenoemd. In toevoeging,wij gevonden Dat de uitdrukking niveaus van ACE2 en IL-6 had a negatieve correlatie met viraal ladingen in COVID-19 patiënten. De negatiefvereniging tussen ACE2 en viraal ladingen kon zijn toegeschreven aan naar dat ACE2 kan verminderen viraal ladingen [39].
interessant genoeg, jonger COVID-19 patiënten hebben a lager immuunrespons en minder viraal ladingen in Immuniteit-M dan ouder patiënten in Immuniteit-H. A potentieel uitleg kon zijn Dat de immuunsysteem is vaak disfunctioneel en heterogeen in ouder mensen[40]. Door veroudering, de immuun systeem vaak veranderingen in twee manieren[40]. Een is immunosenescentie; Dat is, disfunctioneel cellen epigenetisch worden op slot naar binnen a pro-inflliefdesverdriet staat, cytokinen afscheiden en chemokinen. De ander een is inflamm-veroudering ontstaanvan de overactief en niet effectief alarmeren systeem [40]. In toevoeging,wanneer ouderen alveolair TLR's detecteren de pathogeen, zij antwoorden door te produceren type I interferonen tot aantrekken immuun cellen tot de website van infectie. Verder, hoewel de nummer van macrofagen neemt toe met leeftijd, hun plasticiteit tot overzetten tussenpro-enanti-inflliefdesverdriet staten is verminderd [33]. Daarom, de hoger immuunsysteem handtekeningen in Immuniteit-H zijn aannemelijk tot zijn geassocieerd met disfunctioneel immuun reacties in ouder COVID-19 patiënten, lood-ing tot slechter klinisch resultaten, net zo opgemerkt in de vorig resultaten.Daarnaast, wij gevonden Dat IFITM3, a gen spelen a kritisch rol in promoting de immuun systeem's verdediging tegen virussen, wasaanzienlijk gedownreguleerd in COVID-19 versus influenza en RSV-patiënten. Opnieuw, het suggereert een onvoldoende immuun antwoord in COVID-19 versus influenza en RSV patiënten, hoewel de niveaus van pro-inflliefdesverdriet cytokinen zijn opmerkelijk hoger in COVID- 19 dan in influenza en RSV patiënten.
In toevoeging tot de paden van immuun reacties, meerdere metabolic paden waren ontregeld in COVID-19 patiënten. deze metabolische paden zijn betrokken in de abnormaal werkzaamheid vandemitochondriaal ademhalings ketting, negatief regulatie van signalering receptor werkzaamheid, ontregeling van extracellulair Matrix verbindend,ontregeling van nucleoside fosfaat katabolisch werkwijze, regulatie van cytokinese, en chemotaxis, regulatie van TOR signalering,en afgenomen pulmonaal functie. Deze gegevens kunnen uitleggen waarom veel? COVID-19 patiënten tentoongesteld erge, ernstige cardiovasculair en pulmonaal blessure [41]. Bovendien, de extracellulair Matrix regulering is verrijkt in meerdere COVID-19 patiënten, welke Toneelstukken a van vitaal belang rol in vestiging en onderhouden immuun homeostase [42]. Ook,wij gevonden a krachtig correlatie tussen metabolisch ontregeling enimmunogeneticain COVID-19 patiënten. Voor voorbeeld, de verrijking niveaus van MHC klas 1 waren positief gecorreleerd met verminderde pulmonaal functie, extracellulair Matrix verbindend,abnormaal werkzaamheid van mitochondriaal ademhalings ketting, afwijking van de diafragma, positief regulatie van DNA metabolisch werkwijze,en negatief regulatie van ToR signalering. In contrast, zij waren negatief gecorreleerd met de regulatie van positief chemotaxis.Regulatie van positief chemotaxis en positief regulatie van cytokinese was negatief geassocieerd met meest van de 27immuun handtekeningen, terwijl de abnormaal werkzaamheid van de mitochondriaal ademhalings ketting was positief geassocieerd met a meerderheid van deze immuun handtekeningen (Aanvullend Afb. S2).
Ons resultaten ook liet zien Dat sommige COVID-19 patiënten had een sterkere immuun antwoord dan ander COVID-19 patiënten, terwijl deze patiënten vaak had meer erge, ernstige klinisch resultaten. De belangrijkste reden kon zijn Dat hun hyperinflliefdesverdriet reactie tot SARS-CoV-2 infectie, bekend net zo cytokine storm [43 44], resulteerde in in echt orgaan schade. Daarnaast, ons resultaten liet zien Dat ACE2 uitdrukking niveaus waren signifischuin lager in immuniteit-H dan in immuniteit-M en immuniteit-L. Het duidt op Dat ACE2 opregulering zou kunnen lood tot antiviraal immunosuppressie tot oorzaak a slechter prognose in COVID-19 patiënten [45,46].
Hoewel ons studie voorziet in a krachtig baseren voor verder onderzoek naar binnen verschillend immunologisch profiles van COVID-19, influenza,en RSV patiënten, het zou moeten zijn dat is genoteerd Dat deze studie heeft meerdere beperkingen. Eerst, daar zijn insuffiwetenschappelijk klinisch gegevens (e.g., ernst van de ziekte) geassocieerd met ons analyseert, vooral voor influenza en RSV patiënten. Seconde, deze studie was uitgevoerd zonder conopzij zetten de patiënten' onderliggende ziekte geschiedenis vanwege tot beperkt gedetailleerd gegevens verkrijgbaar. Eindelijk, deze studie's onderliggende vooroordeel aan het studeren ontwerp, geduldig populaties, bron weefsels, en technische fouten kan niet zijn regeerde uit net zo residu verwarrend. Echter, onze gegevens nog altijd voorzien in a Doorzichtig in zicht naar binnen de verschil in immuunreacties tussen COVID-19, influenza, en RSV patiënten. De signeefischuin verschillend immuun reacties in verschillend COVID-19patiënten kon zijn aansprakelijk voor signifischuin verschillend klinisch resultaten tussen COVID-19 gevallen. 5. Ethiek goedkeuring en toestemming tot deelnemen
Ethisch goedkeuring en toestemming tot deelnemen waren afgezien sinds we gebruikt enkel en alleen publiekelijk verkrijgbaar gegevens en materialen in deze studie.

6. Toestemming voor publicatie
Niet van toepassing.
Financiering
Deze werk was ondersteund door de Wetenschap en Technologie Project van traditioneel Chinese Geneesmiddel in Zhejiang Provincie (studiebeurs nummer: 2017ZKL003).
Credit auteurschap bijdrage uitspraak
Zeinab Abdelrahman: conceptualisatie, Methodologie, Software, Geldigmaking, Formeel analyse, Onderzoek, Gegevens curatie,visualisatie, Schrijven - origineel voorlopige versie. Zuobing Chen: Methodologie, Software, Geldigmaking, Formeel analyse, Onderzoek, Gegevens curaties, visualisatie, Financiering acquisitie. Haoyu Lyu: Software,Geldigmaking, Formeel analyse, Onderzoek, Gegevens curatie, visualisatie. Xiaosheng Wang: conceptualisatie, Methodologie,Bronnen, Onderzoek, Schrijven - opnieuw bekijken & bewerken, Overzicht,Project administratie, Financiering acquisitie.
Verklaring van Concurreren Interesse
De auteurs verklaren Dat zij hebben nee bekend concurrerend financiaal interesses of persoonlijk verhoudingen Dat kon hebben scheen te influence de werk gemeld in deze papier.
Dankbetuigingen
Niet verkrijgbaar.
Bijlage A. Aanvullend gegevens
Aanvullend gegevens tot deze artikel kan zijn gevonden online Bijhttps://doi.org/10.1016/j.csbj.2021.04.043.
Referenties
[1] Centrum, J.H.C.R. COVID-19 Kaart. 2020; Verkrijgbaar van: https://coronavirus.jhu.edu/kaart.html.
[2] Cao B, Wang Y, wen D, Liu W, Wang J, Fan G, et al. A Proces van Lopinavir-Ritonavir in volwassenen Opgenomen in het ziekenhuis met Erge, ernstige Covid-19. N Engels J Med 2020;382 (19):1787–99. https://doi.org/10.1056/NEJMoa2001282.
[3] Z. Abdelrahman M. Li X. Wang 11 10.3389/fimmu.2020.552909 10.3389/fimmu.2020.552909.s001.
[4] Molenaar C, O'Sullivan J, Jeffrey J, Stroom D. brachiaal plexus neuropathie Tijdens de COVID-19 Pandemie: A Retrospectief Geval Serie van 15 Patiënten in Kritieke zorg. fysio daar. 2021;101(1):pzaa191. doi:10.1093/pzaa191.
[5] schachten GD. COVID-19 versus de 1918 influenza pandemie: verschillend virus,verschillend leeftijd sterfte patronen. J Reis Med. 2020;27(5):taaa086.doi:10.1093/functie/taaa086.
[6] Li M, Zhang Z, Cao W, Liu Y, doe B, Chen C, et al. identificeren roman geassocieerde factoren met COVID-19 overdragen en fataliteit gebruik makend van de machine learning nadering. wetenschap Totaal omgeving 2021;764:142810. https://doi.org/ 10.1016/j.scitotenv.2020.142810.
[7] Langfelder P, Horvath S. WGCNA: een R pakket voor gewogen correlatie netwerk analyse. BMC Bio-informatica. 2008;9:559. gepubliceerd 2008 december 29.doi:10.1186/1471-2105-9-559.
[8] Tufan A, Avano![]() lu Güler A, Matucci-Cerinic M. COVID-19, immuun systeem reactie, hyperinflammatie en herbestemming antireumatisch drugs. Turk J
lu Güler A, Matucci-Cerinic M. COVID-19, immuun systeem reactie, hyperinflammatie en herbestemming antireumatisch drugs. Turk J
Med wetenschap. 2020;50(SI-1):620-632. gepubliceerd 2020 april 21. doi:10.3906/doorzakken- 2004-168.
[9] Della-Torre E, Campochiaro C, Cavalli G, de Luca G, Napels A, La Marca S,et al. Interleukine-6 blokkade met sarilumab in erge, ernstige COVID-19 longontstekingmet systemisch hyperinflammatie: een open-label cohort studie. Ann Rheum Dis2020;79(10):1277–85. https://doi.org/10.1136/annrheumdis-2020-218122.
[10] Giamarellos-Bourboulis EJ, Netea MG, Rovina N, Akinosoglou K, Antoniadou A,Antonakos N, et al. Complex Immuun ontregeling in COVID-19 Patiënten met Ernstig Ademhaling Mislukking. Cel Gastheer Microbe 2020;27(6):992– 1000.e3. https://doi.org/10.1016/j.chom.2020.04.009.
[11] Ragab D, Salah Eldin H, Taeimah M, Khattabu R, Salem R. De COVID-19Cytokine Storm; Wat Wij Weten Dus Ver. Voorkant Immunol. 2020;11:1446.gepubliceerd 2020 juni 16. doi:10.3389/fimmu.2020.01446.
[12] Lieberman DUTJE, Peddu V, Xie H, et al. In levend antiviraal gastheer transcriptionele respons tot SARS-CoV-2 door viraal laden, seks, en leeftijd. PLoS Biol. 2020;18(9): e3000849. gepubliceerd 2020 september 8. doi:10.1371/logboek.bio.3000849.
[13] Arunachalam PS, Wimmers F, Mok CKP, Perera RAPM, Scott M, Hagan T, et al.Systemen biologisch beoordeling van immuniteit tot mild versus erge, ernstige COVID-19infectie in mensen. Wetenschap 2020;369(6508):1210–20. https://doi.org/ 10.1126/wetenschap:abc6261.
[14] Mick E, Kam J, Pisco AO, et al. Bovenste luchtwegen gen uitdrukking onderscheidt COVID-19 van ander acuut ademhalings ziektes en onthult onderdrukking van aangeboren immuun reacties door SARS-CoV-2. Voordruk. medRxiv 2020;2020(05). https://doi.org/10.1101/2020.05.18.20105171. gepubliceerd 2020 Kunnen 19.
[15] Overmyer KA, Shishkova E, Molenaar IJ, Balnis J, Bernstein MN, Peters-Clarke TM,et al. Groot-Schaal Multi-omic Analyse van COVID-19 Ernst. Cel Syst. 2021;12 (1):23–40.e7. https://doi.org/10.1016/j.cels.2020.10.003.
[16] Altman MC, Baldwin N, Walvis E, et al. A transcriptoom Vingerafdrukken Assay voor. Klinisch Immuun Toezicht houden. 2019:587295.
[17] Herberg JA, Kaforou M, Gormley S, et al. transcriptomisch profileng in jeugd H1N1/09 influenza onthult verminderd uitdrukking van eiwit synthese genen. J Infecteren Dis. 2013;208(10):1664-1668. doi:10.1093/indexen/jit348
[18] Bonifacius A, Tischer-Zimmermann S, Draak AC, Gussarow D, Vogel A, Krettek U, et al. COVID-19 immuun handtekeningen onthullen stal antiviraal T cel functioneren ondanks afnemend humoristisch reacties. Immuniteit 2021;54(2):340–354.e6. https://doi.org/10.1016/j.immuun.2021.01.008.
[19] Laing AG, Lorenc A, Del Molino Del Barrio I, et al. A dynamisch COVID-19 immuun handtekening omvat verenigingen met arm prognose [gepubliceerd correctie verschijnt in nat Med. 2020 september 9;:] [gepubliceerd correctie verschijnt in nat Med.
2020 december;26(12):1951]. nat Med. 2020;26(10):1623-1635. doi:10.1038/ s41591-020-1038-6.
[20] Paget C, Trottin F. COVID-19, enflu: geconserveerd of specific immuun handtekening?. Cel Mol Immunol 2021;18(2):245–6. https://doi.org/10.1038/ s41423-020-00595-3.
[21] Hij Y, Jiang Z, Chen C, Wang X. Klassiekfikation van verdrievoudigen-negatief borst kanker gebaseerd Aan immunogenomisch profileng. J Exp Clin Kanker Onderzoek. 2018;37(1):327.gepubliceerd 2018 december 29. doi:10.1186/s13046-018-1002-1.
[22] Hänzelmann S, Castelo R, Guinney J. GSVA: gen set variatie analyse voor microarray en RNA-volgende gegevens. BMC Bio-informatica. 2013;14:7. gepubliceerd 2013Jan 16. doi:10.1186/1471-2105-14-7.
[23] Subramanisch A, Kuehn H, Gould J, Tamayo P, Mesirov JP. GSEA-P: a desktop applicatie voor Gen Set verrijking Analyse. Bio-informatica 2007;23 (23):3251–3. https://doi.org/10.1093/bio-informatica/btm369.
[24] Hoffmann M, kleine-Weber H, Schröder S, Krüger N, Herrler T, Erichsen S,et al. SARS-CoV-2 Cel binnenkomst Hangt ervan af Aan ACE2 en TMPRSS2 en Is Geblokkeerd door een klinisch Bewezen protease remmer. Cel 2020;181(2):271–280.e8. https:// doi.org/10.1016/j.cel.2020.02.052.
[25] Knaus WA, Draper EA, Wagner DP, Zimmerman JE. APACHE II: a ernst van ziekte klassiekfikation systeem. Kritiek Zorg Med. 1985;13(10):818-829.
[26] Charlson MIJ, Pompei P, Ales KL, MacKenzie CR. A nieuwe methode van classificeren van prognostische comorbiditeit in longitudinaal studies: ontwikkeling en geldigmaking. J Chronische Dis 1987;40(5):373–83. https://doi.org/10.1016/0021-9681(87) 90171-8.
[27] Terpos E, Ntanasis-Stathopoulos I, Elalamy I, et al. hematologisch findings en complicaties van COVID-19. Ben J hematol 2020;95(7):834–47. https://doi.org/ 10.1002/ajh.25829.
[28] Pavia BIJ. virale infecties van de lager ademhalings traktaat: oud virussen, nieuwe virussen, en de rol van diagnose. Clin Infecteren Dis 2011;52(Supplement 4): S284–9. https://doi.org/10.1093/cid/cir043.
[29] Newton AH, Cardani A, Braciale TJ. De gastheer immuun antwoord in respiratoir virus infectie: balanceren virus opruiming en immunopathologie. SeminImmunopathol 2016;38(4):471–82. https://doi.org/10.1007/s00281-016-
[30] Asakawa S, Namkoong Ho, Mitamura K, Kawaoka Y, Saito F. Co-infectie met SARS-CoV-2 en influenza A virus. gevallen 2020;20:e00775. https://doi.org/ 10.1016/j.idcr.2020.e00775.
[31] Schwartz DA, Dhaliwal A. INFECTIES IN ZWANGERSCHAP MET COVID-19 ENANDERE ADEMHALINGS-RNA VIRUS ZIEKTEN ZIJN ZELDENALS OOIT,VERZONDEN TOT DE FOETUS: ERVARINGEN MET CORONAVIRUSSEN, HPIV,hMPV RSV, EN INFLUENZA [gepubliceerd online vooruit van afdrukken, 2020 april 27].Boog Pathol Laboratorium Med. 2020;10.5858/arpa.2020-0211-SA. doi:10.5858/arpa.2020-0211-SA.
[32] Grifoni Alba, Weiskopf Daniela, Ramirez Sydney I, Mateus Jose, Dan Jennifer M,Modebacher Caroline Rydyznski, et al. doelen van T Cel Reacties tot SARS-CoV-2 Coronavirus in mensen met COVID-19 Ziekte en Niet-blootgestelde personen. Cel 2020;181(7):1489– 1501.e15. https://doi.org/10.1016/ j.cel.2020.05.015.
[33] Winkler ES, Bailey AL, Kafai NM, et al. SARS-CoV-2 infectie van menselijk ACE2-transgeen muizen oorzaken erge, ernstige long inflammatie en verzwakt functie[gepubliceerd correctie verschijnt in nat Immunol. 2020 september 2;:]. nat Immunol. 2020;21(11):1327-1335. doi:10.1038/s41590-020-0778-2.
[34] Kreijtz JH, Fouchier RA, Rimmelzwaan vriendin. Immuun reacties tot influenza-virus infectie. Virus Onderzoek 2011;162(1–2):19–30. https://doi.org/10.1016/j. virusres.2011.09.022.
[35] Lukens Michael̈l V, bestelwagen de Pol Alma C, Coenjaerts Frank EJ, Jansen Nicolaas JG,Kamp Vera M, Kimpen Jan LL, et al. A systemisch neutrofiel antwoord gaat vooraf aan robuust CD8(plus)T-cel activering gedurende natuurlijk ademhalings syncytieel virale infectie in zuigelingen. J Virol 2010;84(5):2374–83. https://doi.org/10.1128/ JVI.01807-09.
[36] Welliver Timoteüs P, Garofalo Roberto P, Hosakote Yashoda, hints Karen H,Avendano Luis, Sanchez Katherine, et al. Erge, ernstige menselijk lager ademhalings ziekte van de luchtwegen veroorzaakt door ademhalings syncytieel virus en influenza virus is gekarakteriseerd door de afwezigheid van pulmonaal cytotoxisch lymfocyt reacties. J Infecteren Dis2007;195(8):1126–36. https://doi.org/10.1086/52247510.1086/512615.
[37] Russell CD, Unger SA, Walton M, Schwarze J. De Menselijk Immuun Antwoord naar Ademhaling syncytieel Virus Infectie. Clin microbiologisch Rev 2017;30(2):481–502. https://doi.org/10.1128/CMR.00090-16.
[38] Osin´ska I, Popko K, Demkow U. Perforin: een belangrijk speler in immuunrespons. Cent EUR J Immunol. 2014;39(1):109– 15. https://doi.org/10.5114/ ceji.2014.42135.
[39] Monteil Vanessa, Kwon Hye-soo, Prado Patricia, Hagelkrüja Astrid, Wimmer Reiner A, Stahl Martin, et al. remming van SARS-CoV-2 infecties in Gemanipuleerde mens Weefsels Gebruik makend van Klinisch-Cijfer Oplosbaar Menselijk ACE2. Cel 2020;181 (4):905–913.e7. https://doi.org/10.1016/j.cel.2020.04.004.
[40] Mueller Amber L, McNamara Maeve S, Sinclair David A. Waarom doet COVID-19onevenredig beïnvloeden ouder mensen?. Veroudering (Albany New York). 2020;12 (10):9959–81. https://doi.org/10.18632/veroudering.v12i1010.18632/veroudering.103344.
[41] Gardinassi LG, Souza COS, verkoop-Campos H, Fonseca SG. Immuunen metabolisch Handtekeningen van COVID-19 Onthuld door transcriptomics Gegevens Hergebruik.Voorkant Immunol. 2020;11:1636. gepubliceerd 2020 juni 26.doi:10.3389/fimmu.2020.01636.
[42] Li Geng, Fan Yaohua, Lai Yanni, Han Tiantian, Li Zonghui, Zhou Peiwen, et al.Coronavirus infecties en immuun reacties. J Med Virol 2020;92 (4):424–32. https://doi.org/10.1002/jmv.v92.410.1002/jmv.25685.
[43] Yazdanpanah Fereshteh, Hamblin Michael R, Rezaei Nima. De immuunsysteem en COVID-19: vriend of vijand?. Leven wetenschap 2020;256:117900. https://doi. org/10.1016/j.lfs.2020.117900.
[44] Liedje CY, Xu J, Hij JQ, Lu YQ. Immuun disfunctie volgend COVID-19,vooral in erge, ernstige patiënten. wetenschap vertegenwoordiger. 2020;10(1):15838. gepubliceerd 2020 september28. doi:10.1038/s41598-020-72718-9.
[45] Al-Benna Sammy. Vereniging van hoog niveau gen uitdrukking van ACE2 in vetweefsel met sterfte van COVID-19 infectie in zwaarlijvig patiënten. zwaarlijvigheid Med. 2020;19:100283. https://doi.org/10.1016/j.geobsedeerd.2020.100283.
[46] Wang Q, Zhang Y, Wu L, Niu S, Liedje C, Zhang Z, Lu G, Qiao C, Hu Y, Yuen KY,Wang Q, Zhou H, Yan J, Qi J. Structureel en Functioneel Basis van SARS-CoV-2binnenkomst door Gebruik makend van Menselijk ACE2. Cel. 2020 Kunnen 14;181(4):894-904.e9. DOI: 10.1016/j.cel.2020.03.045. epub 2020 april 9. PMID: 32275855; PMCID:
PMC7144619.
